Розсіяний склероз: невирішені проблеми та сучасні підходи у діагностиці та лікуванні

Незважаючи на низку досліджень, у теорії розсіяного склерозу залишається багато проблем, без вирішення яких неможливий подальший прогрес у діагностиці та лікуванні. Вимагають висвітлення багато питань патогенезу цієї хвороби та слід розробити напрями подальших досліджень, результати яких дозволили б оптимізувати існуючі діагностичні та терапевтичні алгоритми.
Розсіяний склероз (РС) — поширене аутоімунне захворювання нервової системи, яке є важливою медико-соціальною проблемою сучасності. Незважаючи на велику кількість публікацій і досягнутий прогрес у розумінні його патогенезу, залишається багато важливих питань, на які досі не отримано вичерпну відповідь. В останнє десятиліття спостерігається невідповідність між досягненнями мікробіології та імунології в області РС та діючими клінічними рекомендаціями щодо ведення пацієнтів.
Тут ми висвітлимо деякі сучасні аспекти патогенезу цього захворювання та важливі перспективні напрямки досліджень, результати яких сприятимуть оптимізації діагностичних та лікувальних підходів.
Розсіяний склероз є поліетіологічним захворюванням, яке розвивається як взаємодія між імунною системою і зовнішніми факторами у генетично сприйнятливих людей. Існує дедалі більше доказів, що віруси можуть відігравати певну роль у патогенезі РС, діючи як зовнішні пускові тригери. Однак невідомо, чи один вірус є причиною РС, чи кілька вірусів можуть одночасно бути поштовхом до розвитку захворювання.
Сучасні вчені розглядають зв’язок різних вірусів з РС, акцентуючи увагу на двох різновидах вірусів герпесу: вірусі Епштейна-Барра (EBV) та вірусі герпесу людини 6 типу (HHV-6). В останні роки дослідниками було відзначено, що ці два агенти мають найбільший вплив як можливі ко-фактори розвитку хвороби.
Одним з найважливіших фактів, що підтверджує зв’язок EBV з РС, є коморбідність симптомів, характерних для інфекційного мононуклеозу та персистуючого хронічного процесу, викликаного EBV та HHV-6, а також дані серологічних досліджень та виявлення вірусного навантаження у хворих на РС. Однак відомо, що симптоми мононуклеозу можуть бути викликані іншими представниками герпес-групи. HHV-6 значно частіше виявляється у бляшках РС, на відміну від EBV, порівняно з результатами досліджень нервової тканини мозку — білої речовини здорових людей.
Також відмічається активація HHV-6 під час загострень РС. Вірусне навантаження герпес-вірусами, насамперед EBV і HHV-6, мононуклеарних клітин периферичної крові виявилося значно вищим у пацієнтів з РС, ніж у групі контролю, і поєднувалося зі змінами в деяких показниках клітинного та гуморального імунітету, суттєво підвищуючись у періоди рецидивів хвороби.
Інфекційна етіологія РС обговорюється фахівцями понад сто років. За цей час із цим захворюванням пов’язували велику кількість вірусів, а також інших інфекційних агентів. Асоціація захворювання з вірусом, звичайно, не означає простого прямого причинно-наслідкового зв’язку, і насправді уявлення або припущення про більшість ймовірно-асоційованих агентів не витримали випробування часом. Наприклад, вірус кору вважали тісно пов’язаним з РС у минулому, але введення вакцинації проти кору не мало впливу на поширеність РС у популяції. Однак накопичені протягом часу дані свідчать про значну роль зовнішніх факторів, таких як віруси, у патогенезі РС. Останніми роками багато авторів знову звертаються до інфекційної теорії патогенезу РС, проте не як єдиного чинника, а як частини складнішого етіологічного процесу, у якому генетична схильність, імунологічні порушення, інфекційні втручання відіграють певну роль. Висновки про те, що генетичні чи епігенетичні фактори не можуть повністю пояснити розвиток та прояви РС у монозиготних близнюків, знову вказали на важливість впливу факторів навколишнього середовища на патогенезі цього захворювання.
Найбільше даних за останні кілька років накопичилося щодо важливої ролі у патогенезі цього захворювання вірусу Епштейна-Барра (EBV) і вірусу герпесу людини 6 типу (HHV-6). Інші асоційовані агенти включають вірус вітряної віспи (VZV), цитомегаловірус (CMV), герпес простий 1 типу (HSV-1) та ендогенні ретровіруси людини (HERV). Однак до теперішнього часу прямий причинно-наслідковий зв’язок жодного з асоційованих агентів із захворюванням РС не виявлено.
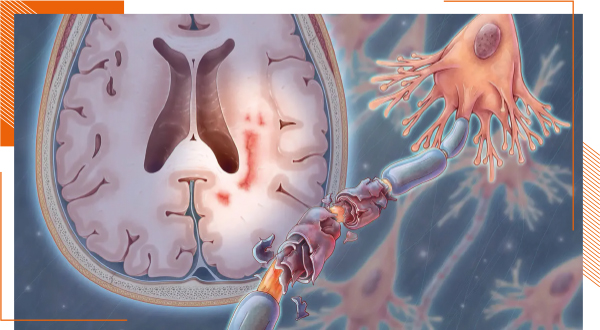
Чим більше ми розуміємо механізми патогенезу РС, тим ясніше, що це захворювання насправді є мультифакторіальною проблемою з генетичними, зовнішніми та імунологічними компонентами. Ступінь взаємодії цих факторів потребує додаткових досліджень. Гетерогенність проявів захворювання змушує припустити, що РС не викликається лише одним вірусом, але скоріше — складнішим комплексом вірусних інфекцій, які можуть діяти як тригери у генетично сприйнятливих осіб. Багато питань потребують додаткового вивчення: генетична схильність, рівні вітаміну D, інтенсивність УФ-опромінення, куріння та наявність вірусних агентів — їх комплексний вплив посилює ризик розвитку РС чи всі ці фактори існують незалежно? Відповіді на ці питання ведуть до більш глибокого розуміння можливих механізмів впливу вірусів на розвиток РС. Крім того, дослідження поширеності у популяції у світі певних вірусів, асоційованих з РС, допоможуть встановити зв’язок із поширеністю самого захворювання у певних регіонах, посилюючи доказову базу вірусної природи у патогенезі даного захворювання.
Нами розглянуто останні дані щодо досліджень зв’язку інфекційних агентів з РС, основними з яких є EBV та HHV-6. Найбільш вагомим із доказів, що пов’язують EBV з РС, є значно більший відсоток пацієнтів із серологічним підтвердженням активності вірусу та вірусного навантаження у крові пацієнтів із цим захворюванням порівняно з контрольною групою того ж віку. Висновки щодо EBV є досить однорідними у літературі, тоді як для HHV-6 спостерігається велика різнорідність у дослідженнях, які демонструють достовірно більш високі показники титрів антитіл HHV-6 та вірусного навантаження у пацієнтів із РС, ніж у групі контролю. Це, ймовірно, відображає відсутність надійних, перевірених та комерційно доступних серологічних тестів для HHV-6. Дійсно, більшість серологічних даних, що свідчать про зв’язок між HHV-6 і РС, були отримані з використанням «домашніх», специфічних для окремої лабораторії, методів, які важко відтворити та які потребують додаткових умов при проведенні аналізу. Навпаки, на відміну від EBV, ДНК HHV-6, РНК і білки, що відповідають за реплікацію вірусу, частіше виявлялися в різних рідин організму, зокрема в тканинах мозку у пацієнтів з РС, ніж в здорових людей контрольної групи.
Крім перегляду асоціації вірусів з РС, ми пропонуємо нову стратегію для оцінки ролі інфекційних агентів у даній патології. Ця стратегія включає розробку актуальних протоколів обстеження хворих, проектування клінічних випробувань з ефективними противірусними та імунобіологічними препаратами, а також високочутливих та об’єктивних принципів ідентифікації активності асоційованих збудників.
Механізми участі вірусів у патогенезі РС
Більшість даних, що зв’язують РС з вірусом (або вірусами), базувалися на визначенні наявності частини вірусу, такої як ДНК, РНК або білків, в рідинах або тканинах організму, а також імунної відповіді на вірус. Імунна відповідь на віруси включає, в основному, дослідження антитіл у сироватці або лікворі пацієнтів з РС, порівняно з результатами, отриманими у відповідних контрольних групах. Відповіді Т-клітин на різні віруси також були вивчені, хоча і меншою мірою. Контрольні групи пацієнтів, які брали участь в різних дослідженнях, варіюють і найчастіше включають здорових людей. Однак умовно здорові суб’єкти, можливо, не є найбільш інформативною контрольною групою, у той час як доцільно розглядати ближчі групи пацієнтів, наприклад, хворих на інші запальні неврологічні розлади. Такі дослідження дали б велику кількість ймовірно асоційованих з РС агентів, але мало відомо про те, як саме віруси причетні до захворювання, механізм їх впливу, а також те, як вони перешкоджають моделюванню процесу хвороби РС.
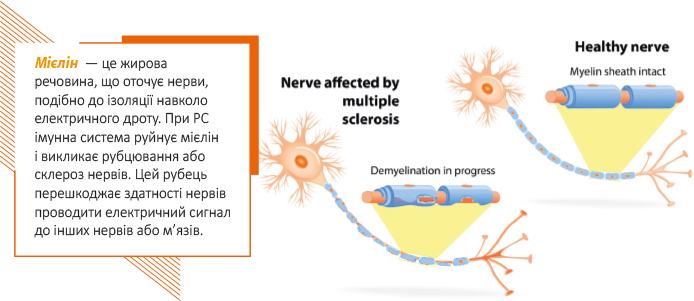
Незважаючи на те, що сучасний погляд на патогенез РС наголошує на ролі імунологічних механізмів, не можна виключити пряму загибель мієлінутворюючих олігодендроцитів або пряму вражаючу дію активної вірусної інфекції в клітинах ЦНС. Можливо, імунна активація та інфільтрація лімфоцитами бляшок при РС є вторинним ефектом через активну вірусну інфекцію в олігодендроцитах або, ймовірно, в інших резидентних клітинах ЦНС. Пряма вірусна інфекція олігодендроцитів може дійсно спричинити загибель клітин та демієлінізацію. Відомо, що хронічна вірусна інфекція ЦНС може викликати захворювання та демієлінізацію. При підгострому склерозуючому панцефаліті (SSPE) хронічна повільна інфекція ЦНС, викликана вірусом кору, призводить до запального процесу як сірої, так і білої речовини головного мозку.
Вперше було зазначено, що РС може бути асоційований з вірусом кору, оскільки у пацієнтів найчастіше виявляють аномально високий титр антитіл до цього вірусу. Сьогодні для багатьох це видається застарілим фактом, проте дослідження, проведені останнім часом, знову привернули увагу до даної асоціації. Існує думка, що найвищий титр антитіл до вірусу кору у пацієнтів з РС може бути наслідком поліклональної активації В-лімфоцитів під впливом EBV. Саме EBV розглядають як основний тригер РС. Однак накопичилося багато даних про роль інших вірусів герпесу — HHV-6 та VZV. Рідше «провокатором» хвороби може бути M. pneumonie, а ще рідше — ендогенні ретровіруси. Навпаки, СMV інфекція асоційована зі зниженим ризиком розвитку РС. Подібний позитивний вплив раніше описано для HHV-7 щодо синдрому Веста у дітей. Відносно новими даними є докази залученості HSV-1 до розвитку РС. Описано як безпосередній вплив вірусу, так і опосередкований — через активацію інших інфекційних агентів, особливо ретровірусів. Таким чином, РС є гетерогенним станом провокуючих факторів. Можливо, саме це визначає клінічну неоднорідність самого РС.
Головним механізмом зриву імунної толерантності вважають молекулярну мімікрію антигенних мікробних агентів під молекули мозку, але ступінь такої мімікрії, як і задіяні антигенні детермінанти, істотно відрізняються залежно від інфекції. У той час, показано, що інфекційні чинники не тільки запускають, а й підтримують аутоімунну реакцію при РС.
Хоча деякі вчені вважають, що РС може бути викликаний одним вірусом, клінічна гетерогенність цього захворювання та різноманітність бляшок РС у ЦНС свідчить про те, що у патогенезі цього захворювання може брати участь більше одного інфекційного агенту. Крім того, визнання можливої ролі більш ніж одного інфекційного тригера у розвитку РС принаймні частково пояснює чисельний список вірусів, які пов’язують з розвитком цього захворювання (табл. 1).
Таблиця 1
Частковий перелік вірусів, які пов’язували з РС за роками
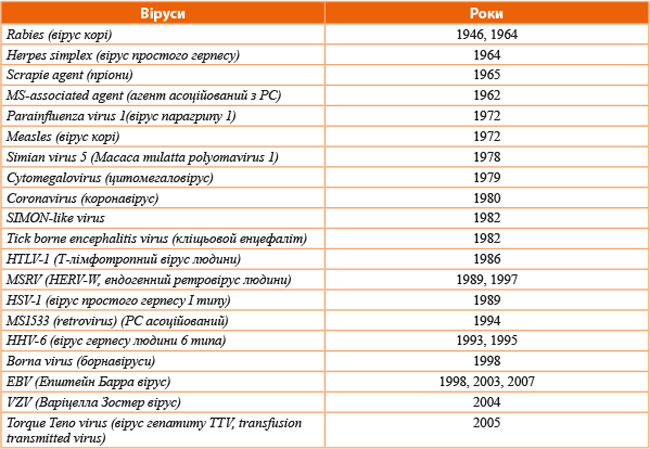
Так, продемонстровано, що реактивація вірусів герпесу збігається із загостреннями хвороби. Поки що накопичено мало даних про вплив цього мікробного агенту на клінічну картину та перебіг РС. Однак є підстави вважати, що вірус кору викликає переважно первинно-прогресуючі форми хвороби, а EBV і HHV-6 асоційовані з рецидивуючим-ремітуючим перебігом РС. Тим не менш, при HHV-6 інфекції більша частота атипових форм хвороби, аніж при EBV. VZV, ймовірно, асоційований з вторинно-прогресуючим РС. Невідомо, як впливають на РС M. pneumonie, ретровіруси та комбінації мікроорганізмів. Якщо ці дані будуть підтверджені та доповнені у подальших дослідженнях, можна буде створити класифікацію РС залежно від інфекційного фактору. Описано також випадки зворотного зв’язку — реактивації герпес-вірусів під впливом РС, наприклад, активації HSV-1 з гассерового ганглію у вигляді herpes labialis при демієлінізації в ділянці трійчастого нерву.
Не слід забувати, що не лише аутоімунний процес, а й самі віруси здатні індукувати демієлінізацію, вражаючи шванівські клітини та індукуючи запальну реакцію. Так, описані непоодинокі випадки мультифокального демієлінізуючого лейкоенцефаліту, викликаного HHV-6 та EBV, які було важко диференціювати від РС. VZV-васкулопатія дрібних церебральних судин також нагадує РС за нейровізуалізаційними ознаками, хоча осередки при цій патології є лакунарними інфарктами, а не бляшками демієлінізації.
Нами описано реактивовану VZV-інфекцію у молодого пацієнта з послідовним ураженням спинного мозку, церебральних судин та зорового нерву, що значною мірою нагадує РС. Існують повідомлення про мультифокальний демієлінізуючий енцефаліт, викликаний HSV-1, який імітував РС за клінічними симптомами, МР ознаками та протіканням. Випадки ретробульбарного невриту описані при EBV та HHV-6 інфекції. Деякі дослідники рекомендують розрізняти вірусні та аутоімунні загострення при РС, особливо при HHV-6 інфекції, що важливо для підбору адекватної терапії. Автори описали поєднання РС з HHV-6 лейкоенцефалітом, причому останній імітував екзацербацію аутоімунної хвороби. Крім того, ураження, пов’язані з VZV-васкулопатією, можуть формуватися на тлі існуючого РС, що ускладнює діагностику. Як показує практика, у пацієнтів з РС усі наявні симптоми зазвичай автоматично пов’язують саме з аутоімунним процесом, ігноруючи клініко-інструментальні прояви можливої вірусної нейроінфекції. Необхідно розробити чіткі критерії диференціальної діагностики вірусних та аутоімунних атак при РС, що неможливо без раціонального використання мікробіологічних та імунологічних досліджень.
Імунологічні дослідження
Наріжним каменем діагностики аутоімунних хвороб вважають проведення імунологічних тестів, що виявляють специфічний субстрат аутоімунної реакції — аутоантитіла та аутореактивні клітини. На сьогодні при РС не використовують імунологічні тести, а діагноз встановлюють лише за клініко-інструментальними даними. Цим пояснюються численні діагностичні помилки.
Сьогодні опубліковано багато робіт, у яких аналізують найбільш типові помилки в діагностиці РС. Нейроімунологи виділяють основні та другорядні інфекційні захворювання, які часто плутають з РС. До перших відносять хворобу Віппла, нейроборреліоз, сифіліс, ВІЛ-енцефалопатію, бруцельоз, HHV-6 лейкоенцефаліт, гепатит С, мікоплазмовий енцефаліт та хворобу Крейтцфельдта-Якоба, а до інших — хворобу кошачої рикетсіозної етіології та лептоспіроз мозку. Не слід також забувати про прогресуючу мультифокальну лейкоенцефалопатію, спричинену JC вірусом. Описано випадок HTLV-1 нейроінфекції, що нагадує РС. Є повідомлення про менінгоенцефаліт, викликаний вірусом Коксакі групи В, який був схожим на РС. Більше того, навіть системна HSV-2 інфекція може нагадувати РС та бути причиною діагностичної помилки.
До неінфекційних хвороб, що мають подібні до РС клініко-інструментальні ознаки, слід віднести антифосфоліпідний синдром, нейроформу синдрому Шегрена, оптичну невропатію Лебера, параінфекційні неврологічні ураження, целіакію, полігландулярний аутоімунний синдром, адренолейкодис.
Запропоновано спеціальний термін «хвороба, що нагадує РС» (multiple sclerosislike disease), який охоплює всі випадки різних захворювань, при яких часто помилково встановлюють діагноз РС. Тільки використання імунологічних тестів, що об’єктивізують специфічний субстрат аутоімунної реакції при РС, дозволить уникнути численних діагностичних помилок та зволікань із призначенням адекватної терапії.
На сьогодні відомо принаймні три механізми аутоагресії при РС, кожен з яких може бути оцінений лабораторними дослідженнями. Ці тести доступні в Україні, проте їх часто не використовують. Класичним є Th1-опосередкований шлях, пов’язаний з аутоантитілами до основного білку мієліну, який закінчується реакцією антитілозалежної цитотоксичності в тканини ЦНС. Пізніше буловідкрито Th17-опосередкований механізм, у результаті чого в мозку накопичуються сенсибілізовані нейтрофіли. Також у патогенезі РС беруть участь специфічні цитотоксичні CD8+ Т-лімфоцити. Є підстави вважати, що кожен механізм по-своєму впливає як на характер вогнищ демієлінізації на МР-знімках, так і на протікання і прогноз хвороби, і навіть на чутливість до препаратів терапії, модифікуючі протікання РС.
Однак ці зв’язки ще потрібно вивчити, оскільки наявних даних замало для висновків. Коли такі зв’язки будуть детально охарактеризовані, ми матимемо кілька інформативних діагностичних та прогностичних лабораторних тестів при РС. Імунологічні тести дозволяють встановити первинний імунодефіцит, ускладненням якого може бути РС. Деякі фахівці розглядали РС як мультиспецифічну імунодефіцитну хворобу ще в 1977 року.
Теорія імунодефіциту може пояснити сімейні випадки РС, дебют хвороби в молодому віці, реактивацію опортуністичних мікроорганізмів, поєднання з іншими аутоімунними розладами, наприклад, бульозним пемфігоїдом, та чутливість до імунотерапії. Іноді самі імунодефіцити імітують РС, що може спричинити діагностичну помилку. Описано EBV позитивну первинну лімфому ЦНС у монозиготних близнюків із загальним варіабельним імунодефіцитом, яку було важко відрізнити від РС за клініко-нейровізуалізаційними ознаками. Є відомості про множинні осередкові ураження мозку при хронічній гранулематозній хворобі, дуже схожі на такі при РС. Описано також мультифокальну демієлінізацію при мутації TNFRSF1A R92Q та синдромі Muckle-Wells. Множинні осередки демієлінізації, спричинені HHV-6, можуть спостерігатися у пацієнтів з дефіцитом мієлопероксидази фагоцитів.
Якщо говорити про зв’язок вторинних імунодефіцитів і РС, слід виділити дефіцит вітаміну D, що призводить до дисфункції регуляторних Т-клітин і підвищеного ризику аутоагресії. Сьогодні рекомендують приймати вітамін D3 і кальцій як допоміжну терапію при РС. У той же час ВІЛ може імітувати РС шляхом індукції мультифокальної енцефалопатії.
Таким чином, впровадження імунологічних тестів допоможе в діагностиці та лікуванні РС відразу на кількох рівнях, тому проведення подальших досліджень у цьому напрямі дуже перспективне та актуальне.
Сучасні підходи до лікування
Незважаючи на успішну апробацію великої кількості препаратів, на сьогоднішній день саме β-інтерферони та глатірамера ацетат є основою профілактичної терапії РС.
Ефективність глатірамера ацетату не перевищує 30-40 %, а його механізм дії пов’язаний із впливом лише на одну ланку патогенезу — опосередковану з Th1.
Бета-інтерферони впливають відразу на два механізми — Th1-опосередкований, зменшуючи проникність гематоенцефалічного бар’єру та змінюючи експресію ряду прозапальних субстанцій, та Th17-індукований, пригнічуючи накопичення сенсибілізованих нейтрофілів у тканині ЦНС. Очевидно, ці відмінності пояснюють вищу ефективність β-інтерферонів як засобів базисної терапії РС, за даними деяких досліджень, що досягає 60-70 %. Нещодавно встановленим механізмом імуномодулюючого впливу β-інтерферонів є пригнічення експресії TLR 9, що бере участь у патогенезі РС. Однак механізм дії цих препаратів може бути ширшим, ніж стверджують нині. Так, існує низка публікацій, що вказують на прямий противірусний ефект β-інтерферонів по відношенню до герпетичних агентів у пацієнтів із РС. Більше того, у хворих, які приймають ці препарати, знижується частота та тяжкість ГРВІ, що вказує на ширший противірусний потенціал терапії. T. Petersen та співавтори продемонстрували пригнічення ендогенних ретровірусів HERV-H та HERV-W у пацієнтів з РС під впливом препарату β-інтерферону. Також було показано, що прямий противірусний ефект β-інтерферонів залежно від умов експерименту в 10-100 разів вищий, ніж у α-інтерферонів, які є загальновизнаними противірусними агентами. Про ефективність β-інтерферонів при дефіциті природних кілерів стало відомо ще у 80-х роках минулого сторіччя. Була виявлена здатність HHV-6 пригнічувати продукцію ендогенних β-інтерферонів в організмі людини. Тому такі препарати можна розглядати і як протимікробні агенти, і як засоби базисної терапії імунодефіциту, що лежить в основі багатьох випадків РС. У той же час, не зрозуміла ефективність β-інтерферонів при РС, індукованому мікоплазмовою інфекцією, апріорі менш чутливою до подібної терапії, ніж герпес-віруси. Очевидно, раціональне використання мікробіологічних та імунологічних досліджень дозволить покращити підбір засобів терапії, що модифікує перебіг РС, який сьогодні проводять емпірично.
Останнім часом відмічається тривожна тенденція до повернення до імуносупресивних методів профілактичного лікування РС, які зазнали фіаско в недавньому минулому, поступившись місцем імунотерапії. Нові імуносупресивні препарати найчастіше мають швидший ефект, ніж імунотерапевтичні агенти, подібно до глюкокортикоїдів під час загострень. Проте безпека такої терапії є сумнівною, особливо — у довгостроковій перспективі. Про асоціацію прийому наталізумабу з прогресуючою мультифокальною лейкоенцефалопатією стало відомо завдяки спостереженням при РС та хворобі Крона.
Описано випадок скроневого пайового некротично-геморагічного енцефаліту HSV-1 етіології після призначення наталізумабу у тридцятишестирічної жінки з РС. Є повідомлення про HSV-2 менінгіт при прийомі наталізумабу. Більше того, наталізумаб призводить до посилення репродукції HHV-6 в олігодендроцитах хворих на РС через зниження імунного нагляду.
Існують повідомлення про розвиток первинної лімфоми ЦНС у пацієнта з РС, який отримував наталізумаб. Алемтузумаб виявився дещо ефективнішим за β-інтерферон при ремітуючій РС, однак у третині випадків індукував інші аутоімунні ускладнення, найчастіше — тироїдит. Може розвинутись neuromyelitis optica та VZV-менінгіт під впливом мітоксантрону у пацієнта з РС. Тяжкість ускладнень терапії значно перевищувала такі ж самого РС. Описано загрозливий для життя DIHS/DRESS у пацієнта з РС, який приймає мітоксантрон. Як відомо, це ускладнення сьогодні пов’язують із HHV-6 інфекцією. Фінголімод може викликати погіршення клінічної та нейровізуалізаційної картини РС, як було показано у кількох недавніх дослідженнях.
Погіршення стану прийому фінголімоду можливе також внаслідок індукції реактивації герпес вірусів. Ймовірний розвиток VZV-енцефаліту і васкулопатії церебральних судин у пацієнта з РС, який приймав цей селективний цитостатик.
Враховуючи доведену патогенетичну роль деяких інфекційних агентів у патогенезі РС, перспективною є профілактична антимікробна терапія при цій хворобі. У цьому напрямку вже зроблено перші кроки, проте ще мало відомо про ефективність подібного підходу до лікування. Була продемонстрована користь від профілактичної терапії ацикловіром дозою 800 мг тричі на добу у пацієнтів із РС.
Нові досягнення в галузі мікробіології та імунології підривають основи концепції щодо суто аутоімунної природи РС, а також ставлять під сумнів уявлення про цілісність та самостійність хвороби. Виникає справедливе питання: чи є РС справді аутоімунною хворобою чи лише реакцією? Занадто великі відмінності між концентричним склерозом Балло, марбурзьким варіантом і класичним рецидивуючим-ремітуючим РС. Навіть у рамках ремітуючої форми хвороби відзначається широка варіабельність за часом дебюту, частоти та тяжкості нападів, зон ураження нервової системи, клінічних симптомів, наслідків та чутливості до терапії.
Відкриття в галузі мікробіології та імунології пояснюють неоднорідність РС різноманітністю мікробних тригерів, імунопатологічних механізмів та імунодефіцитів, що лежать в основі хвороби. Є підстави вважати, що комплекс проявів, який ми нині називаємо РС, насправді не є однією хворобою, а групою гетерогенних синдромів різних захворювань із подібною клініко-інструментальною картиною. Це пояснило б безпрецедентну неоднорідність РС та неможливість ідентифікації однієї причини хвороби. Подібні зміни сьогодні відбуваються і у вивченні бронхіальної астми. Проте, останні досягнення у розумінні патогенезу РС відкривають нові перспективні шляхи оптимізації діагностики та терапії. У зміні традиційних поглядів немає нічого поганого, якщо ці трансформації ґрунтуються на доказах, адже зрештою ми всі — пацієнти, лікарі та функціонери Міністерства охорони здоров’я — зацікавлені у досягненні прогресу у профілактиці та лікуванні РС, який неможливий без розуміння справжньої природи хвороби. Однак необхідно ще багато попрацювати, щоб поринути у невідомі глибини патогенезу РС.
Тут обговорювалася роль інфекційних агентів, переважно, вірусів у розвитку та патогенезі РС. Незважаючи на наявність зв’язків між РС та кількома вірусами, досі не було доведено, що вірус є причиною цього неврологічного захворювання. Останнім часом переконливі докази зосереджені на членах сімейства герпесвірусів, а саме EBV та HHV-6. Оскільки ці віруси широко поширені серед людства, це створює унікальні проблеми у встановленні причинно-наслідкового зв’язку з цим (або будь-яким іншим) захворюванням. Виділення передбачуваного агенту з тканини ураженого РС, такого як активні бляшки в ЦНС, вірусного навантаження та підвищення гуморальної та клітинної імунної відповіді на ці віруси в периферичній крові та лікворі є сильними аргументами на підтримку цих вірусів як тригерів у процесі захворювання. Зрештою, тільки завдяки добре контрольованим випробуванням противірусного лікування можуть бути встановлені причинний або інший патогенетичний зв’язок цих вірусів та PC.
 08-сен-2024
08-сен-2024